Представьте себе, что ваша иммунная система — это огромная полицейская структура, патрулирующая тело и выслеживающая чужаков вроде вирусов, бактерий и грибков. Однако, как и в любом государстве, нужна контрольная инстанция, следящая за порядком среди самих стражей порядка. Эту роль выполняют специальные клетки, называемые регуляторными Т-клетками.
Именно за изучение этих «контролёров иммунитета» в 2025 году была вручена Нобелевская премия по физиологии и медицине. Награду поделили трое выдающихся учёных: Мэри Брункоу (Mary E. Brunkow), Фред Рамсделл (Fred Ramsdell) и Симон Сакагути (Shimon Sakaguchi). Каждый получил треть общей суммы за вклад в исследование периферической иммунной толерантности.
Симон Сакагути стал первооткрывателем регуляторных Т-клеток, показавшим их важную роль в предотвращении аутоиммунных реакций, когда иммунная система ошибочно атакует здоровые ткани собственного организма. Впоследствии Мэри Брункоу и Фред Рамсделл показали, что нарушение функций этих клеток связано с дефектами в гене Foxp3.
Регуляторные Т-клетки работают как своего рода внутренний контролёр нашей иммунной полиции, удерживая её силы от ненужных нападений на сами себя. Учёные предполагают, что целенаправленное воздействие на эти клетки может стать мощным инструментом против серьёзных болезней, включая аутоиммунные расстройства и даже злокачественные новообразования. Правда, пока подобные методы находятся на этапе экспериментальных клинических испытаний.
Именно за изучение этих «контролёров иммунитета» в 2025 году была вручена Нобелевская премия по физиологии и медицине. Награду поделили трое выдающихся учёных: Мэри Брункоу (Mary E. Brunkow), Фред Рамсделл (Fred Ramsdell) и Симон Сакагути (Shimon Sakaguchi). Каждый получил треть общей суммы за вклад в исследование периферической иммунной толерантности.
Симон Сакагути стал первооткрывателем регуляторных Т-клеток, показавшим их важную роль в предотвращении аутоиммунных реакций, когда иммунная система ошибочно атакует здоровые ткани собственного организма. Впоследствии Мэри Брункоу и Фред Рамсделл показали, что нарушение функций этих клеток связано с дефектами в гене Foxp3.
Регуляторные Т-клетки работают как своего рода внутренний контролёр нашей иммунной полиции, удерживая её силы от ненужных нападений на сами себя. Учёные предполагают, что целенаправленное воздействие на эти клетки может стать мощным инструментом против серьёзных болезней, включая аутоиммунные расстройства и даже злокачественные новообразования. Правда, пока подобные методы находятся на этапе экспериментальных клинических испытаний.
«Нобелевские» исследования
Иммунолог из Японии Симон Сакагути в 1982 году повторил эксперимент, аналогичный исследованию Пенхейла. Удалив тимус трёхдневным самкам лабораторных мышей, он заметил появление признаков воспалительного процесса в яичниках. Однако введение животным Т-клеток с особыми поверхностными маркерами приводило к улучшению состояния здоровья грызунов (Sakaguchi et al., 1982).
Дальнейшие эксперименты позволили биологам определить точные характеристики успокаивающих иммунитет Т-клеток. Оказалось, что это специфический вид лимфоцитов, несущих на своей мембране молекулы CD25 и CD4 одновременно.
Дальнейшие эксперименты позволили биологам определить точные характеристики успокаивающих иммунитет Т-клеток. Оказалось, что это специфический вид лимфоцитов, несущих на своей мембране молекулы CD25 и CD4 одновременно.
CD25 — это часть рецептора к интерлейкину-2, сигнальному веществу, которое воспринимают и некоторые Т-киллеры с CD8 на мембране. Возможно, из-за этого сначала сложилось впечатление, что Т-супрессоры — это лимфоциты с CD8.
В 1995 году Сакагути продолжил свои исследования, детально дополнив предыдущие выводы. В новом эксперименте мышам, лишённым тимуса, вводили либо исключительно лимфоциты с поверхностными маркерами CD25 и CD4 из селезёнок других особей, либо всю популяцию селезёночных клеток, исключая интересующие лимфоциты. Контрольная группа состояла из мышей, которым после операции по удалению тимуса возвращали полный состав донорских селезёночных клеток.
Наблюдения подтвердили, что симптомы аутоиммунных нарушений развивались только у тех животных, которым не ввели необходимые лимфоциты с маркировкой CD25 и CD4. Аналогичным образом отсутствие этих клеток усиливало реакцию отторжения трансплантатов органов от других мышей, демонстрируя их ключевую роль в регуляции иммунного ответа (Sakaguchi et al., 1995).
Наблюдения подтвердили, что симптомы аутоиммунных нарушений развивались только у тех животных, которым не ввели необходимые лимфоциты с маркировкой CD25 и CD4. Аналогичным образом отсутствие этих клеток усиливало реакцию отторжения трансплантатов органов от других мышей, демонстрируя их ключевую роль в регуляции иммунного ответа (Sakaguchi et al., 1995).
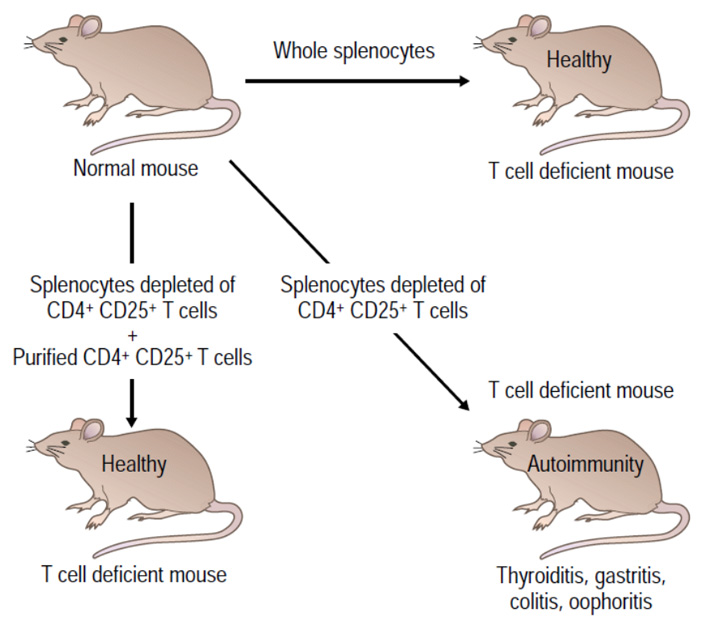
Эксперимент Сакагути 1995 года. Изображение из R. Rich et al (eds). Clinical Immunology: Principles and Practice (Elsevier, 2008. P. 251.)
Экспериментальные животные в исследовании 1995 года подверглись не только утрате тимуса, но и потере соответствующих лимфоидных элементов в периферических отделах иммунной системы, включая лимфатические узлы. Таким образом, у них исчезли собственные лимфоциты, маркированные CD25 и CD4.
Т-лимфоциты с CD4 и CD25 на поверхности получили название регуляторных Т-клеток (Treg). К 2003 году биологи выявили еще одну ключевую молекулярную особенность Treg: в них активен ген Foxp3. Если его «выключить», иммунный ответ организма на свои и чужие структуры усилится.
Ген Foxp3 ранее был обнаружен американскими исследователями Мэри Брункоу и Фредом Рамсделлом совместно с коллегами из компании Celltech Bioscience. Объектом изучения служили мыши с мутацией scurfy («чешуйчатые»), характеризующиеся рядом патологических состояний: поражением кожи, нарушением кроветворения, расстройством пищеварения, проблемами репродуктивной системы и низким весом. Животные погибали вскоре после рождения. У человека аналогичное состояние называется IPEX-синдромом.
Поскольку мутантные самки обычно не демонстрируют выраженных проявлений болезни, исследователи заключили, что мутация затрагивает ген, расположенный на половой X-хромосоме. Определив точную локализацию изменения, авторы присвоили новому гену обозначение Foxp3, а белок-продукт назвали скурфи́н. Позднее выяснилось, что подобный ген существует и у человека, вызывая сходный синдром. (см. C. Bennett et al., 2001. The immune dysregulation, polyendocrinopathy, enteropathy, X-linked syndrome (IPEX) is caused by mutations of FOXP3). Показано, что если доставить в CD4-клетки функциональную копию Foxp3 или «включить» там уже имеющуюся, такие лимфоциты станут регуляторными.
Современная иммунология выделяет целый класс регуляторных Т-клеток, большинство из которых приобретают свои свойства в тимусе, хотя небольшая доля приобретает их вне центральных органов иммунной системы. Более того, есть возможность создавать индуцированные регуляторные Т-клетки «в пробирке».
Т-лимфоциты с CD4 и CD25 на поверхности получили название регуляторных Т-клеток (Treg). К 2003 году биологи выявили еще одну ключевую молекулярную особенность Treg: в них активен ген Foxp3. Если его «выключить», иммунный ответ организма на свои и чужие структуры усилится.
Ген Foxp3 ранее был обнаружен американскими исследователями Мэри Брункоу и Фредом Рамсделлом совместно с коллегами из компании Celltech Bioscience. Объектом изучения служили мыши с мутацией scurfy («чешуйчатые»), характеризующиеся рядом патологических состояний: поражением кожи, нарушением кроветворения, расстройством пищеварения, проблемами репродуктивной системы и низким весом. Животные погибали вскоре после рождения. У человека аналогичное состояние называется IPEX-синдромом.
Поскольку мутантные самки обычно не демонстрируют выраженных проявлений болезни, исследователи заключили, что мутация затрагивает ген, расположенный на половой X-хромосоме. Определив точную локализацию изменения, авторы присвоили новому гену обозначение Foxp3, а белок-продукт назвали скурфи́н. Позднее выяснилось, что подобный ген существует и у человека, вызывая сходный синдром. (см. C. Bennett et al., 2001. The immune dysregulation, polyendocrinopathy, enteropathy, X-linked syndrome (IPEX) is caused by mutations of FOXP3). Показано, что если доставить в CD4-клетки функциональную копию Foxp3 или «включить» там уже имеющуюся, такие лимфоциты станут регуляторными.
Современная иммунология выделяет целый класс регуляторных Т-клеток, большинство из которых приобретают свои свойства в тимусе, хотя небольшая доля приобретает их вне центральных органов иммунной системы. Более того, есть возможность создавать индуцированные регуляторные Т-клетки «в пробирке».
Потенциальные применения
Пока регуляторные Т-лимфоциты не используются широко в клинической практике, их потенциальные возможности активно изучаются. Согласно данным портала clinicaltrials.gov, насчитывается примерно двести зарегистрированных клинических исследований, касающихся применения Treg-клеток, хотя статус ряда проектов остается неопределенным.
Количество и функциональность регуляторных Т-лимфоцитов можно регулировать. Увеличение их числа и активности представляется полезным для лечения аутоиммунных заболеваний, аллергии, а также предупреждения отторжения органов и тканей после трансплантации. Напротив, снижение численности и активности Treg-клеток способно повысить эффективность борьбы с онкологическими заболеваниями.
Для стимуляции активности регуляторных Т-лимфоцитов применяют обработку интерлейкином-2 (IL-2) после предварительного извлечения клеток из организма пациента. Предполагается, что подобная процедура сможет облегчить течение диабета первого типа. Тем не менее проведенное недавно клиническое испытание не подтвердило значимой пользы подобного подхода. Одноэтапное введение расширенной популяции аутологичных регуляторных Т-лимфоцитов показало недостаточную эффективность (Bender et al., 2024).
Тем временем схожий подход оказался успешным при лечении атопического дерматита. Здесь воздействие осуществлялось путем внутривенного введения IL-2 непосредственно пациенту без предварительной экстракорпоральной обработки (Silverberg et al., 2024).
Еще одна интересная стратегия заключается в создании «редактированных» регуляторных Т-лимфоцитов, у которых заменяют рецепторы на нужные варианты, способные взаимодействовать с определенным антигеном. Например, швейцарские ученые успешно испытали подобное вмешательство у мышей с моделью целиакии. Видоизмененные клетки мигрировали в кишечник и подавляли воспалительные процессы, возникающие вследствие употребления глютена (Porret et al., 2025).
Кроме того, доказано, что регуляторные Т-лимфоциты способны способствовать развитию опухолей, подавляя активность клеток иммунной системы, направленных на уничтожение новообразований. Используя моноклональные антитела, нацеленные на рецепторы Treg-клеток, можно снизить их численность и стимулировать антираковый эффект. Эта методика была проверена немецким фармацевтическим концерном Bayer. Применявшееся антитело избирательно истощало популяцию регуляторных Т-лимфоцитов в опухоли, обеспечивая положительный терапевтический эффект (Roider et al., 2024).
Количество и функциональность регуляторных Т-лимфоцитов можно регулировать. Увеличение их числа и активности представляется полезным для лечения аутоиммунных заболеваний, аллергии, а также предупреждения отторжения органов и тканей после трансплантации. Напротив, снижение численности и активности Treg-клеток способно повысить эффективность борьбы с онкологическими заболеваниями.
Для стимуляции активности регуляторных Т-лимфоцитов применяют обработку интерлейкином-2 (IL-2) после предварительного извлечения клеток из организма пациента. Предполагается, что подобная процедура сможет облегчить течение диабета первого типа. Тем не менее проведенное недавно клиническое испытание не подтвердило значимой пользы подобного подхода. Одноэтапное введение расширенной популяции аутологичных регуляторных Т-лимфоцитов показало недостаточную эффективность (Bender et al., 2024).
Тем временем схожий подход оказался успешным при лечении атопического дерматита. Здесь воздействие осуществлялось путем внутривенного введения IL-2 непосредственно пациенту без предварительной экстракорпоральной обработки (Silverberg et al., 2024).
Еще одна интересная стратегия заключается в создании «редактированных» регуляторных Т-лимфоцитов, у которых заменяют рецепторы на нужные варианты, способные взаимодействовать с определенным антигеном. Например, швейцарские ученые успешно испытали подобное вмешательство у мышей с моделью целиакии. Видоизмененные клетки мигрировали в кишечник и подавляли воспалительные процессы, возникающие вследствие употребления глютена (Porret et al., 2025).
Кроме того, доказано, что регуляторные Т-лимфоциты способны способствовать развитию опухолей, подавляя активность клеток иммунной системы, направленных на уничтожение новообразований. Используя моноклональные антитела, нацеленные на рецепторы Treg-клеток, можно снизить их численность и стимулировать антираковый эффект. Эта методика была проверена немецким фармацевтическим концерном Bayer. Применявшееся антитело избирательно истощало популяцию регуляторных Т-лимфоцитов в опухоли, обеспечивая положительный терапевтический эффект (Roider et al., 2024).
Регуляторные Т-клетки и Российские ученые
Безусловно, сегодняшние обладатели Нобелевской премии не являются единственными специалистами, работавшими над проблемой регуляторных Т-лимфоцитов. Одним из наиболее заметных ученых в этой области является выходец из России Александр Руденский. Подобно Сакагути (Hori et al., 2003) и Рамсделлу (Khattri et al., 2003), он также в 2003 году опубликовал статью, подчеркнувшую значимость гена Foxp3 для формирования регуляторных Т-клеток (Fontenot et al., 2003). Стоит отметить, что публикации Руденского и Рамсделла появились в одном выпуске журнала Nature Immunology и расположены на соседствующих страницах издания.
Помимо этого, Руденский, Сакагути и Рамсделл в 2017 году стали лауреатами другого шведского научного признания — премии Крафорда (Crafoord Prize). Данная награда выделяется не в категории «Физиология и медицина», а в специальной номинации, связанной с «исследованиями полиартрита». Этот термин охватывает разнообразные виды воспалительных процессов в суставах, зачастую обусловленных аутоиммунными нарушениями. Причина выделения отдельного направления связана с личным опытом основателя премии Холгера Крафорда, страдающего в поздние годы жизни от ревматоидного артрита.
Известно, что регуляторные Т-клетки (Treg) обладают потенциалом для лечения аутоиммунных заболеваний, что объясняет формулировку премии Крафорда 2017 года: «за открытия, касающиеся регуляторных Т-лимфоцитов, препятствующих аномальным иммунным реакциям при артрите и других аутоиммунных состояниях». Причины, по которым Александр Руденский не вошел в список лауреатов другой премии, присуждаемой Шведской королевской академией наук, остаются неясными. Однако в подробном пресс-релизе о Нобелевской премии текущего года упоминается его научная деятельность, равно как и труды других исследователей в области Treg-клеток.
Помимо этого, Руденский, Сакагути и Рамсделл в 2017 году стали лауреатами другого шведского научного признания — премии Крафорда (Crafoord Prize). Данная награда выделяется не в категории «Физиология и медицина», а в специальной номинации, связанной с «исследованиями полиартрита». Этот термин охватывает разнообразные виды воспалительных процессов в суставах, зачастую обусловленных аутоиммунными нарушениями. Причина выделения отдельного направления связана с личным опытом основателя премии Холгера Крафорда, страдающего в поздние годы жизни от ревматоидного артрита.
Известно, что регуляторные Т-клетки (Treg) обладают потенциалом для лечения аутоиммунных заболеваний, что объясняет формулировку премии Крафорда 2017 года: «за открытия, касающиеся регуляторных Т-лимфоцитов, препятствующих аномальным иммунным реакциям при артрите и других аутоиммунных состояниях». Причины, по которым Александр Руденский не вошел в список лауреатов другой премии, присуждаемой Шведской королевской академией наук, остаются неясными. Однако в подробном пресс-релизе о Нобелевской премии текущего года упоминается его научная деятельность, равно как и труды других исследователей в области Treg-клеток.
